【相變3】從水的相圖看懂固液氣三態轉換
為什麼冰塊會融化成水,水又會變成蒸氣?這些看似平常的現象,其實背後隱藏著物理學中非常有趣的「相變」原理。透過了解物質狀態的改變與相圖,我們能更清楚掌握溫度與壓力如何影響物質的形態,甚至揭露一些生活中不易察覺的特殊現象。
物質狀態轉變的兩大關鍵:溫度與壓力
物質的狀態(固態、液態、氣態)主要由兩個因素控制:溫度和壓力。溫度決定了原子或分子的動能大小,簡單來說,就是它們動得快不快;壓力則像是給這些粒子設下的「活動範圍」,限制它們逃逸的能力。
舉個生活例子:想像你在密閉的熱水瓶裡煮水,裡面的壓力比外面高很多。即使水分子動得很快(高溫),它們也不容易逃逸成氣體,這就是為什麼高壓下水的沸點會比100°C更高。
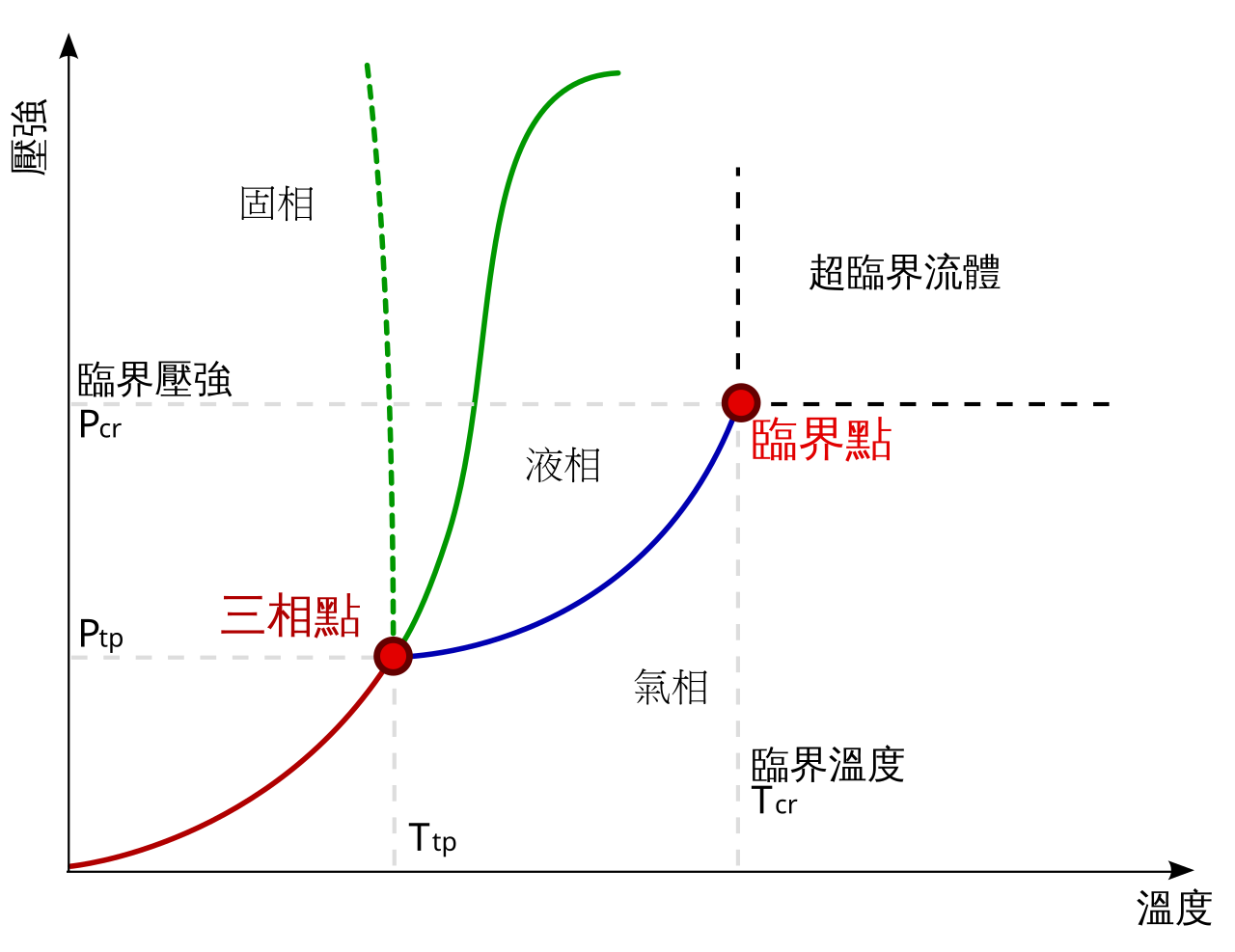
以水的相圖為例:揭示固、液、氣三態的秘密
水是我們日常生活中最常接觸的物質之一,其相圖清楚顯示了不同溫度與壓力下的狀態變化。在標準大氣壓(1 atm)下,水的冰點是0°C,沸點是100°C。這兩個溫度點正是水從固態變成液態,或從液態變成氣態的關鍵轉折。
當壓力改變時,水的相變也會跟著調整。壓力升高,水的沸點會上升,這就是為什麼高山上的水比平地更容易沸騰的原因。更有趣的是,水的冰點在壓力升高時反而會下降,這與大多數物質不同,這種特殊性讓冰在高壓下更容易融化。
特殊的三相點與臨界點
相圖中有兩個非常重要的特殊點:三相點和臨界點。
三相點是指固態、液態和氣態三種形態可以同時共存並達到平衡的條件。對水來說,這個點約在0.01°C和0.006 atm的壓力下。只要維持這個條件,水就會同時存在冰、水和水蒸氣,彼此比例穩定,這是自然界中非常罕見且奇妙的現象。
臨界點則是超過這個溫度和壓力後,液體和氣體的界線消失,物質進入超臨界流體狀態。以水為例,臨界點約在374°C和218 atm。超臨界流體同時具備氣體的擴散性和液體的溶解力,這種狀態在工業和科學研究中有廣泛應用。
潛熱:相變過程中的能量秘密
你可能注意到,當冰融化成水或水變成蒸氣時,溫度並不會立刻改變,但這個過程卻需要大量能量。這就是潛熱的概念。
簡單來說,溫度改變時吸收的能量稱為顯熱,例如將1公斤水加熱1°C需要約4200焦耳的能量。而在相變過程中,物質吸收的能量稱為潛熱,這部分能量用來改變物質的結構,而非溫度。例如,將1公斤100°C的水變成蒸氣,約需100萬焦耳的能量。
二氧化碳的相圖與乾冰現象
除了水,二氧化碳(CO₂)的相圖也很有趣。在標準大氣壓下,CO₂不會有液態,固態的乾冰會直接升華成氣體,這就是為什麼我們看到乾冰會直接變成白霧的原因。
但如果壓力提高,例如達到10 atm,CO₂就會出現固態→液態→氣態的完整轉變過程,並且也有自己的三相點和臨界點,進入超臨界流體狀態,這在工業上有許多應用。
從微觀到宏觀:理解物質狀態轉變的全貌
物質狀態的改變不只是表面現象,微觀層面上是粒子動能和排列方式的改變,宏觀層面則透過相圖和壓力-溫度關係來描述。每當物質從固態變成液態或氣態,物理性質也會隨之轉換,這就是我們所說的相變。
了解這些基本原理,不僅能幫助我們解釋日常生活中的自然現象,也為進一步探索物理學中更複雜的相變現象打下基礎。
透過相圖,我們可以像讀地圖一樣,掌握物質在不同環境條件下的狀態變化,這不僅是科學的美妙,也是生活中的智慧。